问题描述:
已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1×10-12.如图是向10mLAgNO3溶液中逐滴加入0.1mol•L-1NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )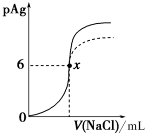
A. 原AgNO3溶液的物质的量浓度为0.1 mol•L-1
B. 图中x点的坐标为(10,6)
C. 图中x点表示溶液中c(Ag+)=c(Cl-)
D. 把0.1 mol•L-1的NaCl溶液换成0.1 mol•L-1的NaI溶液,则图象在终点后变为虚线部分
A.图中原点pAg=0,则Ag+的浓度为:c(Ag+)=100 mol•L-1,即原AgNO3溶液的物质的量浓度为1 mol•L-1,故A错误;
B.x点c(Ag+)=10-6 mol•L-1,一般认为溶液中离子浓度小于10-5 mol•L-1,即沉淀完全,则AgNO3与NaCl恰好反应,n(NaCl)=n(AgNO3)=0.01L×1mol•L-1=0.01mol,所以V(NaCl)=100mL,即x点的坐标为(100,6),故B错误;
C.x点c(Ag+)=10-6 mol•L-1,c(Cl-)=
| 1×10-12 |
| 1×10-6 |
D.与AgCl相比,碘化银的Ksp(AgI)更小,所以把0.1 mol•L-1的NaCl换成0.1mol•L-1NaI,则溶液中c(Ag+)更小,则pAg更大,图象不符,故D错误;
故选C.

