问题描述:
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨的燃烧实验涉及下列两个相关的反应:①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H2
则反应 4NH3(g)+3O2(g)![]() =2N2(g)+6H2O(l) △H= 。(请用含有△H1、△H2的式子表示)
=2N2(g)+6H2O(l) △H= 。(请用含有△H1、△H2的式子表示)
(2)若NH3 ![]() 1/2N2+ 3/2H2 K=a,则N2+3H2
1/2N2+ 3/2H2 K=a,则N2+3H2 ![]() 2NH3 K′= 。(用含a的式子表示)
2NH3 K′= 。(用含a的式子表示)
(3)在体积为3 L的恒容密闭容器中,合成氨N2+3 H![]() 2
2 ![]() 2NH3实验,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如下表所示:
2NH3实验,投入4 mol N2和9 mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如下表所示:
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |
已![]() 知:破坏1 mol N2(g)和3 mol H2(g)中的化学键消耗的总能量小于破坏2 mol NH3(g)中的化学键消耗的能量。
知:破坏1 mol N2(g)和3 mol H2(g)中的化学键消耗的总能量小于破坏2 mol NH3(g)中的化学键消耗的能量。
①则T1 T2(填“>”、“<”或“=”)
②在T2 下,经过10min达到化学平衡状态,则0~10min内H2的平均速率v(H2)= ,平衡时N2的转化率α(N2)= 。
③下列图像分别代表焓变(△H)、混合气体平均相对分子质量(![]() )、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是 。
)、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是 。
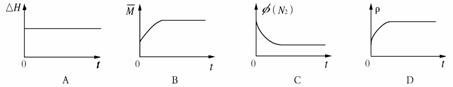
.(1)3/5△H1+2/5△H2
(2)1/a2
(3)①< ② 0.1 mol/(Lmin) 25% ③ BC

